ACC.26 | 中南大学湘雅二医院周胜华、刘启明教授团队:M6A甲基化为连接免疫与特发性肺动脉高压的关键介质
发布于: 2026-04-02
当地时间2026年3月30日,由中南大学湘雅二医院心内科周胜华、刘启明教授团队与湖南省儿童医院心内科肖云彬教授团队联合完成的一项肺动脉高压创新性研究“综合生物信息学分析识别M6A甲基化为连接免疫与特发性肺动脉高压的关键介质”研究(Comprehensive Bioinformatic Analysis Identifies M6a Methylation as a Key Mediator Linking Immunity to Idiopathic Pulmonary Arterial Hypertension)在第75届美国心脏病学会科学年会(ACC.26)上以Moderate Poster发布。团队成员刘娜医生介绍,本研究首次系统揭示了N6-甲基腺苷(m6A)RNA甲基化修饰在特发性肺动脉高压(IPAH)免疫应答调控中的核心作用。该成果为肺动脉高压的发病机制提供了全新的表观遗传学视角,并为开发靶向免疫治疗策略奠定了重要理论基础。
研究背景
肺动脉高压是一种以肺动脉压力升高和小肺血管重构为特征的恶性心血管疾病,目前仍缺乏根治性手段,部分原因在于其病理机制尚未完全阐明。近年来,免疫炎症反应被认为是推动PAH进展的重要因素,但其激活与调控的上游机制一直是科学界关注的焦点。
研究方法及结果
研究团队通过构建野百合碱(MCT)诱导的PAH大鼠模型(图1),结合甲基化RNA免疫沉淀测序(MeRIP-Seq),首次描绘了PAH状态下肺组织m6A甲基化的全景观图谱。结果发现,与对照组相比,PAH大鼠肺组织中m6A修饰水平显著上调,提示m6A修饰异常可能参与PAH的发生发展(图2)。
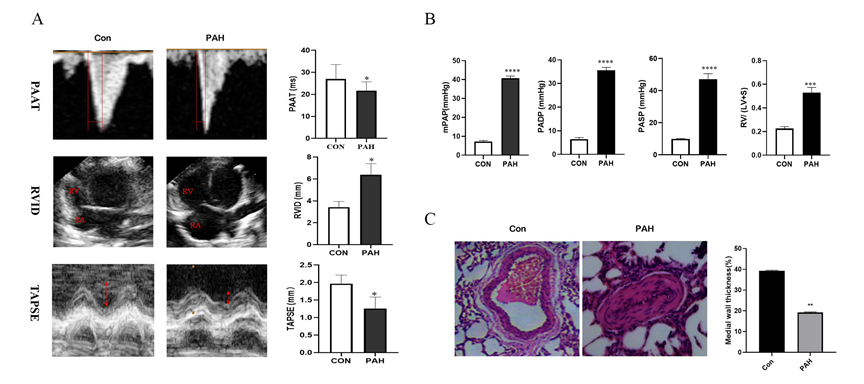
图1:大鼠肺动脉高压(PAH)模型的构建
(A) 超声心动图数据;(B) 血流动力学数据;(C) 显微镜下获取的对照组与PAH组肺动脉HE染色图像。与对照组相比,PAH组可见肺动脉重构。* 表示具有统计学差异。
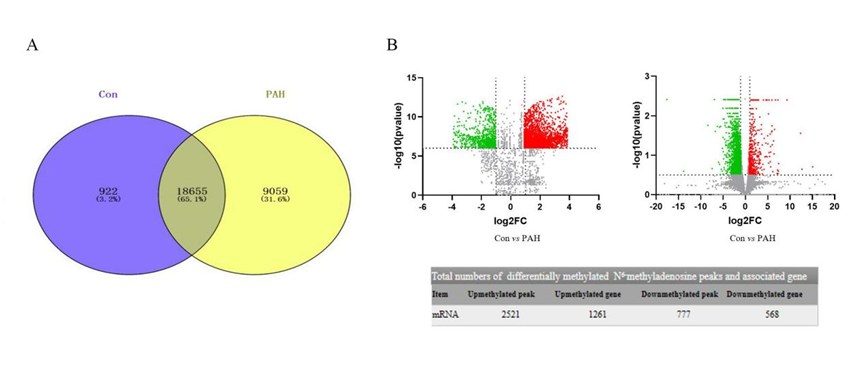
图2:大鼠肺组织甲基化谱
(A)差异m6A甲基化与mRNA甲基化表达统计火山图;绿色表示m6A修饰及mRNA甲基化表达降低,红色则相反。(B) 差异m6A富集峰及相关基因统计图
为了进一步探索m6A修饰与人类特发性PAH的关系,研究团队利用基因表达综合数据库(GEO)中的IPAH患者数据,采用加权基因共表达网络分析(WGCNA)筛选出与m6A甲基化评分密切相关的核心基因模块。通过多列表通路富集分析和蛋白质-蛋白质相互作用(PPI)网络构建,研究团队锁定了一个以趋化因子相关基因为核心的模块,其中CCR5和CXCL9被证实存在显著的m6A上调修饰(图3)。
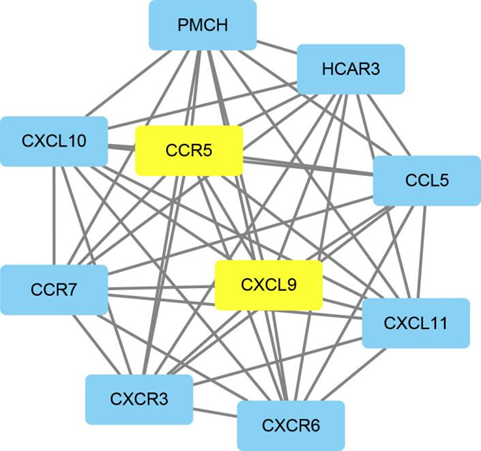
图3:蛋白质相互作用(PPI)分析鉴定的87个甲基化相关基因的关键聚类。
黄色代表高甲基化基因
更为重要的是,研究团队运用CIBERSORT算法对免疫细胞浸润情况进行分析,发现高m6A甲基化评分组中单核细胞向M1型巨噬细胞极化的趋势显著增强。进一步分析表明,这一免疫极化过程可能由m6A修饰调控的CCR5和CXCL9介导。M1型巨噬细胞是促炎反应的核心效应细胞,其异常活化被认为是导致肺血管重构和PAH恶化的重要因素(图4)。
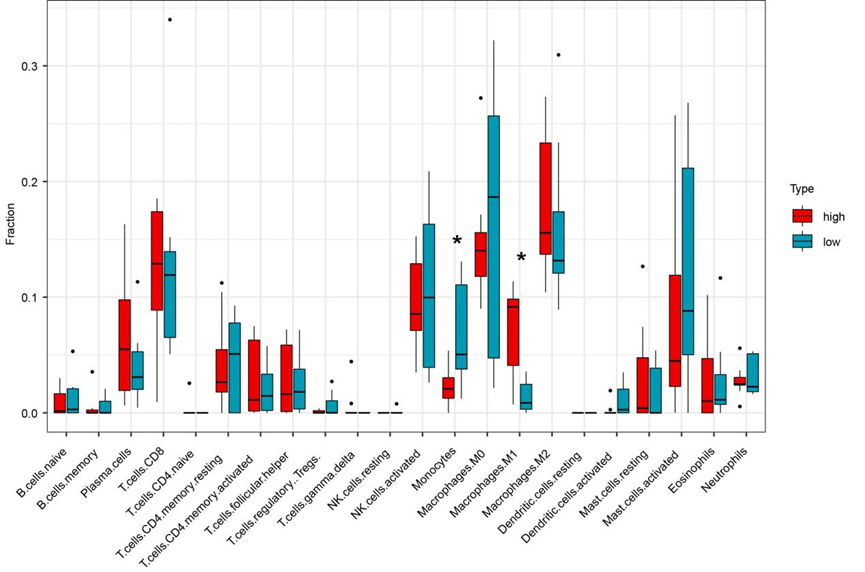
图4: 18例特发性肺动脉高压(IPAH)样本中免疫细胞比例的比例直方图
本研究不仅首次揭示了m6A RNA甲基化在PAH免疫应答调控中的重要作用,还提出了“m6A修饰—趋化因子信号—M1巨噬细胞极化”这一全新的调控轴。这为理解PAH的病理机制提供了新维度,也为未来开发靶向表观转录组或免疫细胞的治疗策略奠定了理论基础。
研究解读
本研究得到了国家自然科学基金、湖南省自然科学基金等多项资助。研究团队表示,下一步将深入探讨CCR5和CXCL9作为m6A下游效应分子的具体调控机制,并探索其在PAH治疗中的应用前景。此项研究不仅填补了m6A修饰在PAH领域的研究空白,也为免疫靶向治疗在心血管疾病中的应用开辟了新的方向。此次研究结果在国际大会上发布,是对团队科研创新和临床研究能力的肯定和鼓舞。
文章作者:刘娜 中南大学湘雅二医院(心血管内科)


